 Complejos de hierro
y azufre
Complejos de hierro
y azufre
Son metaloproteinas cuyo grupo prostético está determinado por un átomo de hierro, pero a diferencia de los citocromos, estos hierros no se encuentran enmarcados en el grupo hemo.
El hierro en estas proteínas se encuentra vinculado a iones de azufre inorgánico como parte de un centro de hierro-sulfuro.
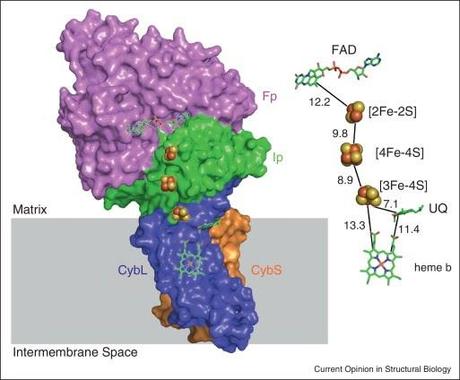
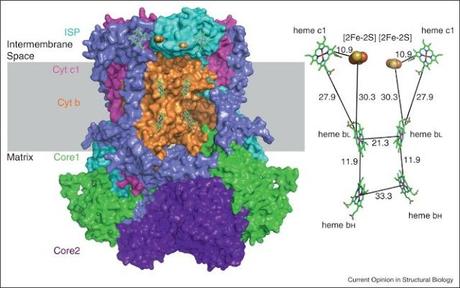
Figura CHS-01. Los grupos prostéticos se encuentran distribuidos a través de la superficie de los complejos de proteínas que componen a la cadena de transporte de electrones, lo suficientemente cerca para que se formen puentes eléctricos entre las posiciones que aceptan y seden electrones. En la imagen se muestra la posición de varios grupos prostéticos de tipo diferente estrechamente unidos entre si.
El centro de hierro-sulfuro más común contiene dos o cuatro átomos de hierro y azufre vinculados a una proteína en los residuos de cisteína.A pesar de que un solo centro puede tener una gran cantidad de átomos de hierro, el complejo completo es capa de transferir un solo electrón por cada ronda redox. El potencial redox de un centro de hierro-sulfuro depende de la carga hidrófoba y la carga de los residuos de aminácidos que rodean al centro de hierro-sulfuro. PRINCIPAL REGRESAR
