Una investigación desarrollada en la Facultad ha comparado niveles de expresión genética en regiones del hipocampo afectadas por la enfermedad
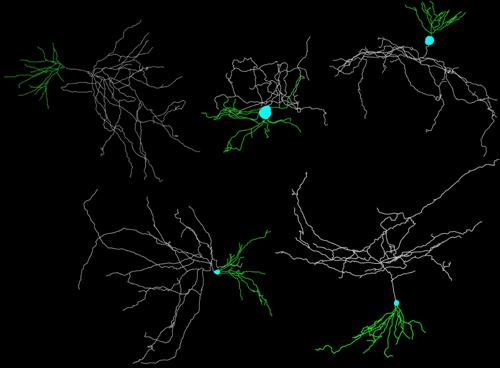
Fig. Reconstrucción de neuronas granulares. Se estima que las neuronas granulares forman el 80% de las neuronas del giro dentado. En contraste, las neuronas piramidales son las más comunes en la corteza entorrinal, constituyendo el grupo de mayor riesgo de lesión en la enfermedad de Alzheimer. Imagen: FIUPM.
8.10.2012. Utilizando técnicas de aprendizaje automático y minería de datos, investigadores del Computational Intelligence Group de la Facultad de Informática de la Universidad Politécnica de Madrid (FIUPM) han comparado los niveles de expresión de los genes de pacientes de Enfermedad de Alzheimer (EA) en dos zonas claves del hipocampo: el giro dentado, donde la enfermedad muestra poca o nula actividad; y, la corteza entorrinal, donde la enfermedad de Alzheimer produce grandes daños neuronales. Los resultados, publicados en Computer Methods and Programs in Biomedicine, corroboran hallazgos previos de otros estudios y plantean nuevas hipótesis de trabajo en la investigación de la EA.Giro dentado y corteza entorrinal
La formación hipocampal es una estructura compleja perteneciente al lóbulo temporal medial del cerebro. Desempeña un papel clave para la memoria, la atención y la orientación espacial. Está compuesta por seis regiones: presubículo, subículo, parasubículo, giro dentado, hipocampo y corteza entorrinal. Destaca, de entre ellas, el giro dentado: una de las pocas regiones del cerebro adulto donde se produce nacimiento de nuevas neuronas (neurogénesis) a lo largo de toda la vida. Se sabe que esta neurogénesis realiza un papel fundamental en la creación de nuevos recuerdos. Estudios histopatológicos postmortem han evidenciado que el giro dentado es la zona hipocampal con menor afectación por parte de la EA.
La corteza entorrinal es el nexo principal entre el hipocampo y la neocorteza. Esta área ejerce un papel clave en la formación y consolidación de recuerdos, así como en la recuperación de recuerdos biográficos, declarativos y espaciales. Hoy en día sabemos que la corteza entorrinal no sólo es una de las primeras áreas en ser afectadas por la EA, sino que es donde mayores lesiones produce su progresión.
Análisis de datos mediante conjunción de clasificadores Bayesianos
La técnica de minería de datos utilizada se enmarca dentro de la disciplina de la Inteligencia Computacional. La potencia de cómputo disponible hoy en día permite analizar grandes cantidades de datos complejos de una manera holística, y así identificar nuevos hallazgos o plantear nuevas hipótesis. Este estudio ha utilizado técnicas estadísticas de conjunción (del inglés ensemble) de modelos matemáticos en la búsqueda de genes relevantes y redes de dependencias entre ellos. En ambos casos, el paradigma matemático utilizado se denomina clasificador Bayesiano.
Resultados
Los resultados señalan genes relevantes en diferentes enfermedades neurológicas, así como los mecanismos metabólicos claves que corroboran hallazgos previos en la investigación molecular de la EA. Uno de estos hallazgos es la desregulación de los genes DEC1 y BTRC, involucrados en la regulación del reloj molecular que controla el ciclo circadiano del cuerpo.
Uno de los síntomas más comunes en la EA es la disfunción del sueño, efecto derivado de la pérdida de referencia circadiana. Los cerebros de los pacientes no identifican correctamente cuando deben dormir o estar despiertos. Los periodos de falta de sueño hacen que la producción de beta amieloide se incremente, haciendo que la enfermedad continúe su progresión.
Otro resultado destacable es la desregulación del gen S100A10. Este gen juega un papel fundamental en los receptores de serotonina cuya actividad está ligada a síntomas neuropsiquiátricos en pacientes con EA.
De igual manera, se sabe que está involucrado en la patogénesis y regulación de desordenes depresivos. Su nivel de actividad diferencial entre giro dentado y corteza entorrinal corrobora estas asociaciones, así como recientes hallazgos que lo identifican como un nuevo biomarcador temprano de la EA.
Referencias
Armañanzas, R., Larrañaga, P. & Bielza, C. (2012). Ensemble transcript interaction networks: A case study on Alzheimer's disease. Computer Methods and Programs in Biomedicine, 108(1), 442-450.
 Posted in: hipocampo,Inteligencia-Computacional,investigacion Alzheimer,neuronas
Posted in: hipocampo,Inteligencia-Computacional,investigacion Alzheimer,neuronas

