El Citomegalovirus humano (CMVH) es un patógeno humano importante que infecta a un gran porcentaje de la población mundial y que supone un alto riesgo para la salud de individuos con el sistema inmune inmaduro o deprimido -recién nacidos, trasplantados o pacientes con Sida-. Conseguir identificar qué proteínas celulares están implicadas en la reproducción viral permitirá tener los elementos necesarios para poder controlar la infectividad de dicho patógeno.
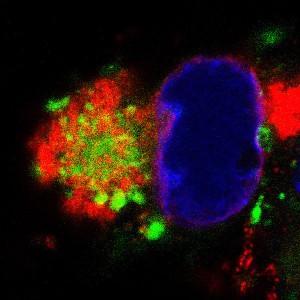
IF de células infectada por CMVH
Al tratarse de un virus rodeado por una envoltura membranosa que proviene de la célula infectada, resulta de interés estudiar las proteínas celulares que están implicadas en procesos de tráfico de membranas. En este sentido, el equipo de investigación del Centro Nacional de Biotecnología dirigido por Alberto Fraile, en colaboración con el grupo del investigador Peter van der Sluijs del Centro Médico Universitario de Utrecht ha demostrado que el virus necesita una proteína que interviene en los procesos de biogénesis y secreción de los denominados Orgánulos Relacionados con los Lisosomas Celulares (ORLs). Concretamente, los autores comprobaron que CMVH induce potentemente la expresión de la pequeña GTPasa Rab27. Cuando se investigó el papel de esta proteína en el ciclo de vida del virus se descubrió que Rab27 era necesaria para la producción de nuevas partículas virales infectivas. Este hallazgo resulta impactante ya que muestra que el CMVH consigue manipular la maquinaria celular implicada en estos procesos para su propio beneficio.
Los ORLs son lisosomas especializados donde se almacena la melanina en los melanocitos o las enzimas líticas en los linfocitos citotóxicos, de manera que mutaciones en el gen Rab27 son responsables del albinismo parcial y de los desordenes del sistema inmune en algunos pacientes con el síndrome de Griscelli. Previamente, los investigadores publicaron que el CMVH adquiere su envoltura de membranas que contienen marcadores celulares tanto de la ruta exocítica como de la ruta endocítica, entre ellos, marcadores de ORLs, lo que ya apuntaba a la existencia de una conexión entre el CMVH y la maquinaria molecular implicada en la biogénesis de estos orgánulos. Según Fraile, se habría dado con la clave a nivel molecular de una ruta celular conservada que es explotada por el virus.
Para llegar a estas conclusiones, los investigadores estudiaron cómo el CMVH induce la expresión de los ARNs mensajeros de Rab27 y de la proteína en las células infectadas. Mediante técnicas de microscopía óptica con marcadores fluorescentes de proteínas, localizaron Rab27 en la zona de ensamblaje viral o factoría viral -auténtica fábrica de virus maduros e infectivos-, y mediante técnicas de microscopía electrónica con marcadores de proteínas acoplados a oro, detectaron Rab27 incorporada en las envolturas virales. Este resultado indica que las membranas celulares que utiliza el CMVH para adquirir su envoltura viral proceden, al menos en parte, de los ORLs. A continuación, estudiaron el efecto del silenciamiento de Rab27 mediante ARNs interferentes en las células infectadas y encontraron que la producción viral se encontraba reducida en las células silenciadas para Rab27. Obtuvieron el mismo resultado cuando utilizaron como sistema modelo al citomegalovirus del ratón y células de ratones deficientes en Rab27, corroborando que la pequeña GTPasa Rab27 está implicada en la producción de las nuevas partículas virales infectivas.
La comprensión de las interacciones virus-célula a nivel molecular es crucial para el desarrollo de nuevos fármacos antivirales. Además, el virus resulta una excelente herramienta para poder comprender la biología celular de estos orgánulos y profundizar en el conocimiento de ciertas patologías humanas, como es el anteriormente mencionado síndrome de Griscelli. Los resultados de este trabajo aparecen publicados en el último número de PLoS ONE.
Ahora, y según Fraile, la cuestión que deberían desentrañar es cómo consigue el virus controlar estos componentes celulares. Puede ser complicado de entender, pero esencial para el desarrollo de uno de los agentes patógenos más extendido en el mundo, terror como infección vírica hospitalaria.
JAL -(CBMSO)
DIVULGACIÓN CIENTÍFICA A 20 DE DICIEMBRE DE 2010
MADRI+D TV (Divulgación científica con cara, e imágenes, en 3 minutos)
ENTRE PROBETAS (Píldoras científicas en 2 minutos). Radio 5
A HOMBROS DE GIGANTES Radio 5
