Sin embargo, el hecho de que algunas sustancias no puedan atravesar espontáneamente la membrana no significa que no puedan hacerlo. La célula posee diferentes tipos de proteínas que pueden actuar como transportadores, con la ventaja añadida para el funcionamiento celular de que tienen carácter específico, es decir, permiten el paso de una sustancia concreta, pero no el de otros compuestos parecidos. Gracias a esto, la célula se mantiene impermeable a compuestos que debe mantener fuera o dentro de ella, pero permite la entrada y la salida de otras sustancias que necesita.
Además, los transportadores de membrana no suelen ser simples conductos "pasivos", sino que en la mayor parte de los casos tienen un estado abierto y otro cerrado, y su apertura o cierre se produce como respuesta a estímulos específicos. De este modo, la célula puede regular la entrada y salida de sustancias entre su interior y el entorno que la rodea, ajustando su funcionamiento a las condiciones externas.
Los iones, debido a su carga eléctrica, son uno de esos tipos de sustancias que atraviesan la membrana con gran dificultad. Aunque la impermeabilidad no es completa, el flujo de iones por difusión a través de la bicapa lipídica es prácticamente nulo. Las proteínas que permiten el paso de ciertos iones de un lado a otro de la membrana reciben el nombre de canales iónicos.
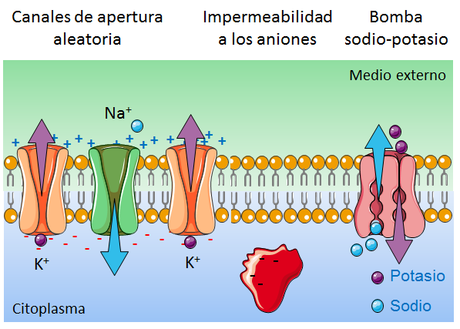
Existen canales para diferentes iones y que responden a distintos tipos de estímulos. Así, los hay que se abren de modo aleatorio, mientras que otros se abren o se cierran como respuesta a un cambio en la diferencia de potencial entre los lados de la membrana (canales operados por voltaje), como resultado de la unión a la proteína de una sustancia química (canales operados por ligando) o incluso como respuesta a un estímulo mecánico, como la presión (canales operados mecánicamente). Muchos de ellos cuando están abiertos simplemente permiten el paso de los iones en ambas direcciones, en cuyo caso el flujo neto se produce según el gradiente de concentración (desde el compartimento más concentrado al más diluido), pero algunos operan en contra de gradiente de concentración, lo que requiere un gasto de energía que, en general, es proporcionado por la hidrólisis del ATP. En este caso estos canales suelen denominarse bombas.
Potencial de reposo
Debido a las propiedades electroquímicas de la membrana y a la actividad de los canales iónicos presentes en ella, se produce una diferencia en el potencial eléctrico entre el citoplasma y el medio extracelular. Esa diferencia de potencial recibe el nombre de potencial de reposo.
El potencial de reposo existe debido a que se produce una cierta acumulación de iones positivos en la cara externa de la membrana y una cierta concentración de iones negativos en la región del citoplasma próxima a la superficie celular. Hay varios factores que contribuyen a explicar esta diferencia en la distribución de cargas eléctricas:
- La distribución desigual de iones entre el interior y el exterior de la célula. El medio extracelular es rico en sodio (Na+) y cloruro (Cl-), mientras que el interior de la célula presenta concentraciones mayores de potasio (K+), fosfato (PO4-3) y aminoácidos. Esta diferencia se debe, al menos en parte, a que la membrana contiene más canales de apertura aleatoria para el potasio que para el sodio, lo que hace que salga de la célula más potasio que el sodio que entra.
- Los aniones intracelulares no pueden atravesar la membrana. Los grupos fosfato y los aminoácidos, que son los aniones más abundantes en el interior de la célula, no pueden atravesar la membrana porque en general se encuentran asociados a moléculas de gran tamaño.
- Existe un sistema activo que mantiene la diferencia de carga. Se trata de la bomba sodio-potasio, una proteína transmembrana que expulsa tres iones de Na+ por cada dos iones de K+ que introduce en la célula. Este sistema funciona en contra del gradiente de concentración, por lo que requiere energía que es proporcionada por la hidrólisis de ATP.
Potenciales graduados
La excitabilidad eléctrica de las neuronas consiste, desde el punto de vista físico-químico, en su capacidad para modificar la diferencia de potencial que existe entre el exterior y el interior de la célula como respuesta a cambios externos.
La llegada de un estímulo hasta la neurona provoca un cambio en su potencial de reposo, al modificar la actividad de algunos canales iónicos. Un potencial graduado es una pequeña desviación del potencial de reposo que puede aumentar (hiperpolarización) o reducir (despolarización) la diferencia de potencial original.
Los potenciales graduados se producen, en general, en las zonas "receptoras" de la neurona, es decir, en las dendritas o en el soma neuronal. Se deben a la activación de canales iónicos operados mecánicamente o por ligando. Se denominan graduados porque la amplitud del potencial depende de la intensidad del estímulo, de modo que estímulos pequeños producen poca variación en el potencial de membrana mientras que estímulos intensos generan mayores variaciones en la diferencia de potencial.
Hay otras dos características importantes de los potenciales graduados. En primer lugar, su intensidad va disminuyendo a medida que nos alejamos del punto donde se ha recibido el estímulo, y en segundo lugar son acumulativos, es decir, pueden sumarse algebraicamente entre sí, lo que significa que potenciales del mismo signo se potencian mientras que potenciales de signo distinto (uno hiperpolarizador y otro despolarizador) tienden a anularse entre sí.
Potencial de acción
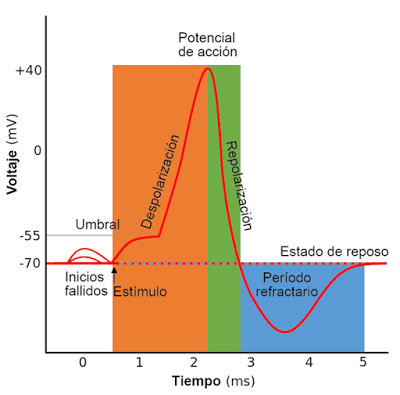 El potencial de acción es una sucesión rápida de procesos que primero reducen y luego invierten el potnecial de reposo de la membrana para finalmente restituirlo a la situación de partida.
El potencial de acción es una sucesión rápida de procesos que primero reducen y luego invierten el potnecial de reposo de la membrana para finalmente restituirlo a la situación de partida.En su desarrollo se distinguen dos fases fundamentales. La primera es la despolarización: el potencial de reposo, de signo negativo (el citoplasma está cargado negativamente respecto al exterior) se invierte hasta alcanzar valores positivos, es decir, hasta que el interior de la célula tiene más cargas positivas que el exterior. A continuación se produce una fase de repolarización, en la que el potencial de membrana vuelve a tomar su valor de reposo. Durante esta fase hay un periodo en el que el potencial de membrana es más negativo que el potencial de reposo (fase de hiperpolarización). Durante la hiperpolarización la membrana no puede generar un nuevo potencial de acción, por lo que este lapso de tiempo se denomina periodo refractario.
El potencial de acción solo se desencadena cuando la diferencia de potencial entre el citoplasma y el exterior alcanza un valor crítico conocido como potencial umbral. Aunque este valor puede variar de unas neuronas a otras, es constante para cada célula y suele ser de unos -55mV frente a los -70mV característicos del potencial de reposo.
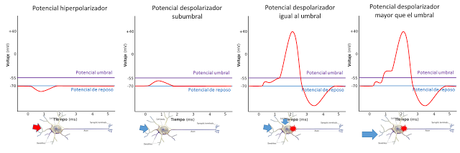
El cambio de potencial de la membrana se produce como respuesta a la llegada de uno o varios potenciales graduados. Si el potencial graduado que alcanza la neurona es hiperpolarizador, o si es despolarizador pero no alcanza el valor umbral, no se desencadena el potencial umbral. En cambio si el potencial graduado alcanza o supera el valor umbral la neurona responde con la generación del potencial de acción. La intensidad de este, una vez que se ha iniciado, es independiente del valor de los potenciales graduados que lo han desencadenado, por lo que se dice que el potencial de acción sigue la "ley del todo o nada".
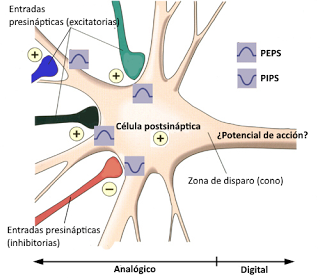
Los potenciales graduados que llegan a la región aferente de la neurona pueden tomar valores diferentes, proporcionales a la intensidad del impulso que los ha provocado, de modo que se puede considerar que la neurona recibe señales "analógicas". La neurona recibe todos esos impulsos y los "integra", sumándolos. Como resultado, solo puede dar dos tipos de respuesta: la generación de un potencial de acción o permanecer inactiva, de modo que se puede decir que la neurona ha transformado múltiples señales de entrada de naturaleza analógica en una única señal de salida de carácter digital.
La generación de un potencial de acción en la membrana de la neurona se debe a cambios en el estado de los canales iónicos operados por voltaje que hay en ella.
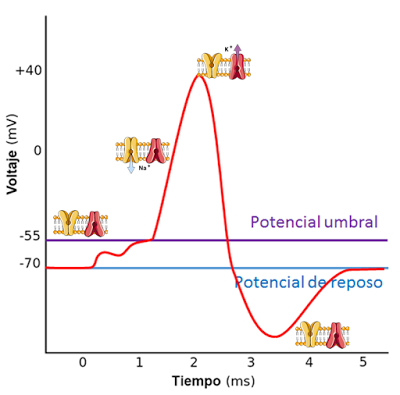 Cuando la célula está en reposo los canales operados por voltaje de sodio y potasio están cerrados. Si la suma de los potenciales graduados que alcanzan la célula iguala o supera el potencial umbral se abren los canales de sodio operados por voltaje, lo que provoca la entrada de este ión hacia el interior de la célula y la despolarización de la membrana.
Cuando la célula está en reposo los canales operados por voltaje de sodio y potasio están cerrados. Si la suma de los potenciales graduados que alcanzan la célula iguala o supera el potencial umbral se abren los canales de sodio operados por voltaje, lo que provoca la entrada de este ión hacia el interior de la célula y la despolarización de la membrana.Cuando se alcanza el potencial máximo, se cierran los canales de sodio y se abren los canales de potasio, lo que provoca la salida de este ión. Los canales de potasio permanecen abiertos incluso después de que se haya recuperado el potencial de reposo, por lo que se produce la hiperpolarización de la membrana.
Finalmente se cierran los canales de potasio, con lo que se recupera el potencial de reposo y la célula vuelve a su estado normal.
La fase de hiperpolarización tiene una importancia fundamental en la transmisión del impulso nervioso. Mientras una zona de la membrana está hiperpolarizada los canales de sodio operados por voltaje presentes en ella no pueden volver a abrirse, de modo que la despolarización solo se transmite en una dirección.
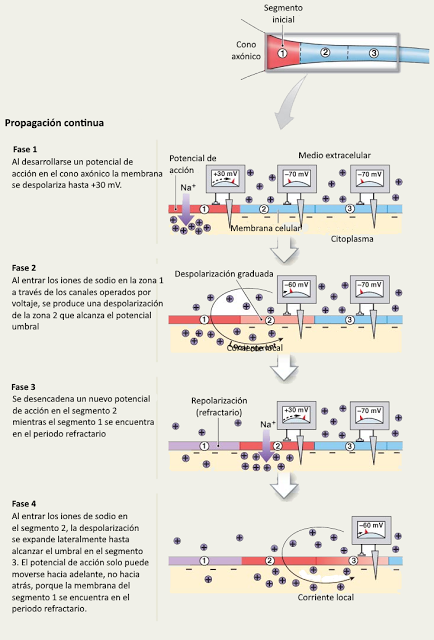 Existen dos modalidades de propagación del impulso nervioso a lo largo de una neurona. La conducción continua se produce en las fibras amielínicas y en las fibras musculares, que también presentan excitabilidad eléctrica. En este caso todos los segmentos de la membrana deben sufrir los procesos de despolarización y repolarización, lo que hace que la transmisión del impulso sea relativamente "lenta".
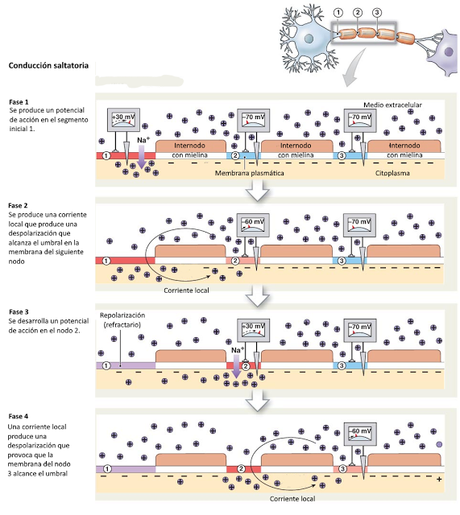
Existen dos modalidades de propagación del impulso nervioso a lo largo de una neurona. La conducción continua se produce en las fibras amielínicas y en las fibras musculares, que también presentan excitabilidad eléctrica. En este caso todos los segmentos de la membrana deben sufrir los procesos de despolarización y repolarización, lo que hace que la transmisión del impulso sea relativamente "lenta".En el caso de las fibras mielínicas, las zonas de la membrana cubiertas por la vaina de mielina no pueden intercambiar iones con el exterior, de modo que estos procesos solo tienen lugar en las zonas en las que la membrana del axón se encuentra "al descubierto", es decir, en los nodos de Ranvier. En los nodos, el potencial de acción se transmite mediante corrientes iónicas locales, que al no necesitar la apertura de canales iónicos, se propagan con mayor rapidez que en el caso de la conducción continua.
Este mecanismo recibe el nombre de conducción saltatoria.
 Codificación de la intensidad de la señal
Codificación de la intensidad de la señalVolviendo a la comparación con sistemas analógicos y digitales, tenemos que las neuronas generan siempre respuestas de la misma intensidad, ya que todos los potenciales de acción son iguales, mientras que la señal que la neurona recibe es analógica, es decir, puede tener diferente intensidad porque puede deberse a estímulos más o menos potentes.
Las neuronas tienen capacidad de ajustar su respuesta a la intensidad del estímulo recibido, fenómeno que se denomina modulación de la respuesta, y lo hacen cambiando la frecuencia con la que emiten los potenciales de acción: a mayor intensidad, mayor frecuencia de respuesta.
Transmisión sináptica
Una sinapsis es la zona donde una neurona se comunica con otra o con una célula efectora. Según el modo en que se establezca esa conexión se distinguen dos tipos de sinapsis.
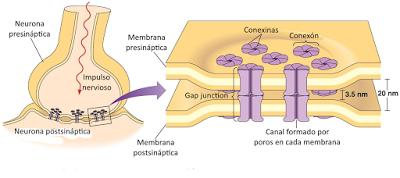 Las sinapsis eléctricas se caracterizan porque la comunicación entre las células se establece mediante un tipo especial de unión intercelular, la gap junction, que consiste en un contacto estrecho entre las dos células de modo que existen canales iónicos operados por voltaje que comunican los dos citoplasmas. De este modo, los iones pueden pasar directamente de la primera célula a la segunda, transmitiendo el potencial de acción de una a la otra. Este tipo de uniones permiten una comunicación rápida, y la sincronización de diferentes neuronas, y son frecuentes en la musculatura visceral y cardíaca, así como durante el desarrollo embrionario, aunque posteriormente van siendo sustituidas por sinapsis químicas.
Las sinapsis eléctricas se caracterizan porque la comunicación entre las células se establece mediante un tipo especial de unión intercelular, la gap junction, que consiste en un contacto estrecho entre las dos células de modo que existen canales iónicos operados por voltaje que comunican los dos citoplasmas. De este modo, los iones pueden pasar directamente de la primera célula a la segunda, transmitiendo el potencial de acción de una a la otra. Este tipo de uniones permiten una comunicación rápida, y la sincronización de diferentes neuronas, y son frecuentes en la musculatura visceral y cardíaca, así como durante el desarrollo embrionario, aunque posteriormente van siendo sustituidas por sinapsis químicas.En las sinapsis químicas no hay continuidad entre las células que se comunican, sino que entre ellas queda un espacio denominado hendidura sináptica. El potencial de acción no puede transmitirse a través de ese espacio, por lo que la comunicación se produce gracias a la participación de una sustancia química liberada por la neurona presináptica, que atraviesa la hendidura sináptica para unirse a receptores específicos de la célula postsináptica y que recibe el nombre de neurotransmisor.
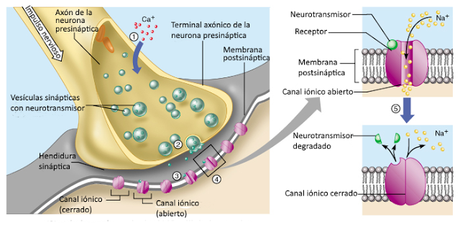
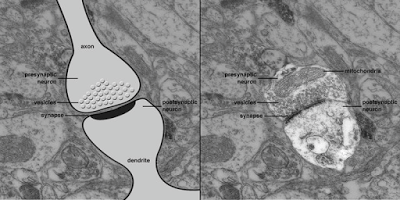 El terminál axónico de la neurona presináptica presenta, en general, un aspecto bulboso y acumula en su interior un considerable número de vesículas de membrana rellenas por el neurotransmisor. La membrana postsináptica, por su parte, presenta un gran número de receptores, proteínas de membrana que se unen específicamente al neurotransmisor,
El terminál axónico de la neurona presináptica presenta, en general, un aspecto bulboso y acumula en su interior un considerable número de vesículas de membrana rellenas por el neurotransmisor. La membrana postsináptica, por su parte, presenta un gran número de receptores, proteínas de membrana que se unen específicamente al neurotransmisor,Cuando el potencial de membrana alcanza el terminal axónico se producen los siguientes procesos:
- La despolarización de la membrana activa canales de calcio operados por voltaje, que permiten la entrada de este ión a la célula.
- Como resultado del aumento del calcio intracelular las vesículas membranosas se fusionan con la membrana presináptica, liberando el neurotransmisor a la hendidura sináptica.
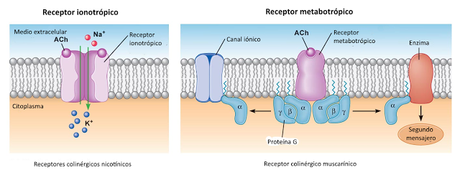
- El neurotransmisor difunde a través de la hendidura, y se une a los receptores de la membrana postsináptica. Estos pueden ser canales iónicos operados por ligando, en cuyo caso se dice que el neurotransmisor es de tipo ionotrópico) que se abren como respuesta a la unión del neurotransmisor.
- La entrada de iones en la célula postsináptica desencadena en ella un potencial graduado. Si el receptor actúa como canal de sodio el potencial es despolarizador, y se denomina Potencial Excitatorio Postsináptico (PEPS), mientras que si se trata de un canal de potasio el potencial postsináptico es hiperpolarizador, y por tanto inhibitorio (PIPS).
Además de los receptores ionotrópicos, que son canales iónicos operados por ligando, existe otro tipo de receptores que reciben el nombre de metabotrópicos. En este caso el receptor no actúa directamente como canal iónico, sino que está asociado a una proteína intracelular (proteína G) que libera en el citoplasma una sustancia que recibe el nombre de segundo mensajero, porque su actividad consiste en "repetir" el mensaje del neurotransmisor, pero en el interior de la célula. Los segundos mensajeros pueden ser de distintos tipos, y pueden tener diferentes efectos, en ocasiones varios a la vez. Entre sus efectos están la activación o inhibición de enzimas o la apertura de canales iónicos, lo que da lugar a potenciales graduados en la célula postsináptica.
 Una vez que el neurotransmisor ha transmitido la señal, ésta debe detenerse para que las células vuelvan a su estado normal. Esto supone que el neurotransmisor debe ser retirado de la hendidura sináptica, lo que puede ocurrir de diferentes formas:
Una vez que el neurotransmisor ha transmitido la señal, ésta debe detenerse para que las células vuelvan a su estado normal. Esto supone que el neurotransmisor debe ser retirado de la hendidura sináptica, lo que puede ocurrir de diferentes formas:- Difusión: el movimiento aleatorio de las moléculas del neurotransmisor hace que se reduzca su concentración en la hendidura sináptica, hasta que ya no llega a provocar un cambio significativo en el potencial de membrana de la célula postsináptica.
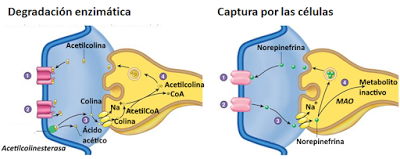
- Degradación enzimática: una enzima situada en la membrana postsináptica rompe el neurotransmisor transformándola en otra molécula inactiva. Un ejemplo de este mecanismo es la destrucción enzimática de la acetilcolina por acción de la acetilcolinesterasa, enzima que la divide en ácido acético y colina. Ambos compuestos son reabsorbidos por la célula presináptica, que los recicla para volver a sintetizar el neurotransmisor.
- Captura por las células: algunos neurotransmisores son recaptados por la célula presináptica o por células de la glía. Una vez en el interior de estas células se inactivan o se reciclan. Un ejemplo de este mecanismo es la recaptación de la norepinefrina.
Existen unas 100 sustancias distintas que ejercen funciones como neurotransmisores en el organismo. Muchas de ellas, además, pueden ser liberadas al torrente circulatorio y actuar como hormonas.
Desde el punto de vista de su estructura química suelen distinguirse dos grandes grupos de neurotransmisores: los neuropéptidos, proteínas formadas por un reducido número de aminoácidos, y otro conjunto de moléculas, químicamente diversas, pero que se incluyen en la categoría de "moléculas pequeñas".
El más conocido de los neurotransmisores es la acetilcolina, que posee receptores metabotrópicos inhibidores e ionotrópicos excitatorios. Se localiza en las neuronas motoras de la médula, en numerosas zonas de la corteza cerebral o en el sistema nervioso autónomo. También hay algunos aminoácidos que desempeñan esta función, como el glutamato, que es el principal neurotransmisor excitatorio de la corteza, el aspartato, la glicina o el GABA (ácido gamma aminobutírico), un aminoácido que no forma parte de las proteínas.
Una tercera categoría de neurotransmisores no proteicos son las aminas biogénicas, que incluyen la adrenalina y la noradrenalina, que son también segregadas como hormonas en las glándulas suprarrenales, la dopamina y la serotonina. Las tres primeras tienen características químicas comunes, y reciben el nombre conjunto de catecolaminas.
Algunos nucleótidos, relacionados químicamente con el ATP (AMP, ADP y ATP) también actúan como neurotransmisores.
Finalmente, dos sustancias bastante peculiares en cuanto a su acción como neurotransmisores son el óxido nítrico (NO) y el monóxido de carbono (CO). Ambas sustancias son gases a temperatura fisiológica, y no se acumulan en vesículas de membrana en las terminaciones axónicas, sino que se producen y liberan al exterior en el momento en el que llega el impulso. Tampoco poseen receptores, ya que pueden atravesar libremente la membrana postsináptica, ejerciendo su función directamente en el interior de la célula.
En cuanto a los neuropéptidos, todos ellos tienen en común ser péptidos de unos 30 a 40 aminoácidos de longitud, que se unen a receptores metabotrópicos. Entre ellos se encuentran los opiáceos endógenos (encefalinas, endorfinas y dinorfinas), que juegan papeles importantes en la detención del dolor, el aprendizaje y la memoria, o el péptido P que, por el contrario, refuerza la sensación de dolor.
El importante papel que juegan los neurotransmisores en la transmisión de la información en las sinapsis ha propiciado que sean uno de los elementos más utilizados para desarrollar tratamientos de las enfermedades que afectan al sistema nervioso. Así, se actúa sobre su proceso de síntesis, ya sea inhibiéndola o estimulándola, como ocurre en el tratamiento de los enfermos de Parkinson con L-Dopa, una sustancia precursora de la síntesis de dopamina. También puede actuarse médicamente sobre su liberación; las anfetaminas, por ejemplo, deben su actividad a que liberan adrenalina y dopamina, mientras que la toxina botulínica actúa bloqueando la liberación de acetilcolina en las neuronas motoras.
Una tercera posibilidad de alterar el funcionamiento de los neurotransmisores es activar o bloquear sus receptores. En el primer caso se utilizan sustancias que se denominan agonistas, porque producen el mismo efecto que el neurotransmisor. Es el caso de los agonistas de la adrenalina y noradrenalina, que se utilizan como broncodilatadores. Por el contrario, las sustancias que provocan los efectos contrarios al neurotransmisor se denominan antagonistas. Los antagonistas de la serotonina y la dopamina se utilizan como tratamientos de la esquizofrenia.
Finalmente, también se puede estimular o inhibir la eliminación del neurotransmisor, reduciendo o aumentando su actividad. La cocaína bloquea la recaptura de la dopamina, por lo que prolonga su efecto, mientras que los inhibidores de la MAO (monoaminoxidasa, enzima que degrada catecolaminas) se usan en el tratamiento de la depresión.
Sumación de estímulos
En general, la llegada de un único potencial presináptico a una neurona puede no ser suficiente para
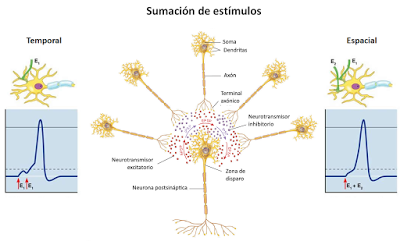 desencadenar un potencial de acción. La respuesta en esta célula puede producirse, en este caso, si se da el fenómeno de sumación de potenciales, que se produce bien cuando varios potenciales graduados procedentes de la misma célula presináptica llegan en un breve periodo de tiempo (sumación temporal) o bien cuando la neurona postsináptica recibe estímulos de diferentes neuronas presinápticas (sumación espacial). Los potenciales graduados que llegan a esta célula pueden ser tanto excitatorios como inhibitorios, de modo que el resultado es la suma neta de todos ellos.
desencadenar un potencial de acción. La respuesta en esta célula puede producirse, en este caso, si se da el fenómeno de sumación de potenciales, que se produce bien cuando varios potenciales graduados procedentes de la misma célula presináptica llegan en un breve periodo de tiempo (sumación temporal) o bien cuando la neurona postsináptica recibe estímulos de diferentes neuronas presinápticas (sumación espacial). Los potenciales graduados que llegan a esta célula pueden ser tanto excitatorios como inhibitorios, de modo que el resultado es la suma neta de todos ellos.Circuitos neuronales
La comunicación entre neuronas no suele ser una a una, es decir, cada neurona recibe información de varias células aferentes y puede enviar información a distintas células eferentes, lo que permite multiplicar las vías y los modos en los que se transmite esa información, de modo que el sistema nervioso funciona como una gran red de enorme complejidad.
Las estructuras básicas de esta red son los circuitos neuronales, conjuntos de neuronas comunicadas entre sí de una forma particular. La arquitectura de cada circuito neuronal. es decir, el modo en el que están conectadas entre sí las neuronas que lo forman, le proporcionan características específicas que le permiten desempeñar funciones concretas dentro del sistema nervioso.
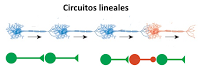 Los circuitos lineales son simplemente cadenas de neuronas dispuestas una tras otra y conectadas secuencialmente entre sí. Si todas las sinapsis son excitatorias la información se propaga sin cambios a lo largo de todo el circuito, mientras que si alguna de las sinapsis es inhibitoria se bloquea o reduce la excitación de neuronas posteriores a lo largo de la cadena.
Los circuitos lineales son simplemente cadenas de neuronas dispuestas una tras otra y conectadas secuencialmente entre sí. Si todas las sinapsis son excitatorias la información se propaga sin cambios a lo largo de todo el circuito, mientras que si alguna de las sinapsis es inhibitoria se bloquea o reduce la excitación de neuronas posteriores a lo largo de la cadena.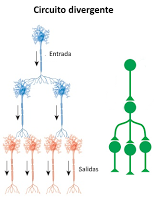
En un circuito divergente una única neurona establece contactos con varias células, lo que permite amplificar su señal y hacer que llegue a varios destinos diferentes. Ejemplos de este tipo de circuitos incluyen los sistemas mediante los cuales un pequeño número de neuronas cerebrales controlan un movimiento corporal estimulando simultáneamente un gran número de neuronas de la médula espinal.
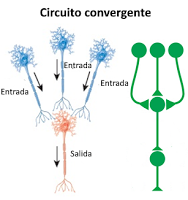
Los circuitos convergentes se establecen cuando una única neurona recibe información de varias células aferentes (presinápticas). Esta estructura permite, por ejemplo, que una única neurona motora reciba información desde neuronas situadas en diferentes partes del cerebro, con lo que el mismo movimiento puede ser realizado como respuesta a distintos estímulos, controlados por cada una de esas partes.
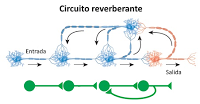 Circuitos reverberantes: en una cadena de neuronas, algunas ramificaciones laterales de las últimas neuronas del circuito activan o inhiben a neuronas anteriores a ellas. Esto permite mantener la respuesta durante periodos considerablemente prolongados, incluso de varias horas, hasta que es detenida por neuronas inhibitorias. Este tipo de circuitos parece jugar papeles importantes en actividades tales como la respiración, el despertar, actividades musculares coordinadas o la memoria a corto plazo.
Circuitos reverberantes: en una cadena de neuronas, algunas ramificaciones laterales de las últimas neuronas del circuito activan o inhiben a neuronas anteriores a ellas. Esto permite mantener la respuesta durante periodos considerablemente prolongados, incluso de varias horas, hasta que es detenida por neuronas inhibitorias. Este tipo de circuitos parece jugar papeles importantes en actividades tales como la respiración, el despertar, actividades musculares coordinadas o la memoria a corto plazo.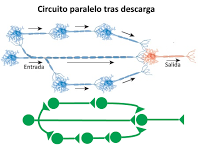 En los circuitos paralelos posdescarga una única neurona presináptica establece conexiones con varias interneuronas, cada una de las cuales conecta con la misma neurona postsináptica después de seguir caminos de diferente longitud. De esta manera la neurona postsináptica puede emitir una sucesión rápida de respuestas como resultado de un único estímulo inicial. Estos circuitos parecen estar relacionados con actividades de precisión, como los cálculos matemáticos.
En los circuitos paralelos posdescarga una única neurona presináptica establece conexiones con varias interneuronas, cada una de las cuales conecta con la misma neurona postsináptica después de seguir caminos de diferente longitud. De esta manera la neurona postsináptica puede emitir una sucesión rápida de respuestas como resultado de un único estímulo inicial. Estos circuitos parecen estar relacionados con actividades de precisión, como los cálculos matemáticos.Regeneración y reparación del tejido nervioso
El sistema nervioso posee una gran plasticidad, es decir, capacidad de cambiar como resultado de la experiencia a lo largo de la vida del individuo. Las manifestaciones de esta plasticidad son la formación de nuevas dendritas, la síntesis de nuevas proteínas y los cambios que tienen lugar en las sinapsis. Sin embargo, su capacidad de regeneración, es decir, de que las neuronas se reproduzcan o se reparen a sí mismas, es muy reducida: en el sistema nervioso periférico puede producirse la regeneración de axones mielinizados dañados si el soma de la célula está intacto y las células de Schwann están activas, pero en el sistema nervioso central se produce muy poca o ninguna regeneración.
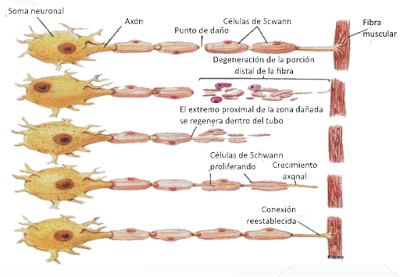 Las neuronas mielínicas del Sistema Nervioso Periférico tienen buenas posibilidades de regenerarse si conservan su soma y el neurolemma, siempre que la cicatrización se produzca a un ritmo lento. Cuando el axón de una de estas células se daña lo primero que ocurre es la degradación de la fibra desde el punto en el que se ha producido la lesión hasta su extremo (degeneración walleriana), debida a la acción de los macrófagos. A continuación las células de Schwann se reproducen y crecen hasta formar un tubo de regeneración, en cuyo interior se produce el crecimiento del axón. Si la distancia entre las células de Schwann que han permanecido intactas es demasiado grande no se produce su proliferación ni la regeneración axonal.
Las neuronas mielínicas del Sistema Nervioso Periférico tienen buenas posibilidades de regenerarse si conservan su soma y el neurolemma, siempre que la cicatrización se produzca a un ritmo lento. Cuando el axón de una de estas células se daña lo primero que ocurre es la degradación de la fibra desde el punto en el que se ha producido la lesión hasta su extremo (degeneración walleriana), debida a la acción de los macrófagos. A continuación las células de Schwann se reproducen y crecen hasta formar un tubo de regeneración, en cuyo interior se produce el crecimiento del axón. Si la distancia entre las células de Schwann que han permanecido intactas es demasiado grande no se produce su proliferación ni la regeneración axonal.En cuanto al Sistema Nervioso Central, hay muchas especies animales, como los pájaros cantores, en los que se producen neuronas nuevas de una manera más o menos constante a lo largo de la vida. En mamíferos este proceso parece estar mucho más limitado, aunque se ha encontrado la formación de nuevas neuronas en algunas zonas del encéfalo como el hipocampo, zona relacionada con el aprendizaje.
El estudio de la regeneración neuronal en diferentes especies muestra patrones de crecimiento diferente en el ser humano y los primates relacionados al compararlos con otros mamíferos como el ratón. En los homínidos la regeneración de las neuronas del giro dentado (hipocampo) es mucho más importante que en otros mamíferos, afectando a la práctica totalidad de la zona a lo largo de la vida del individuo.
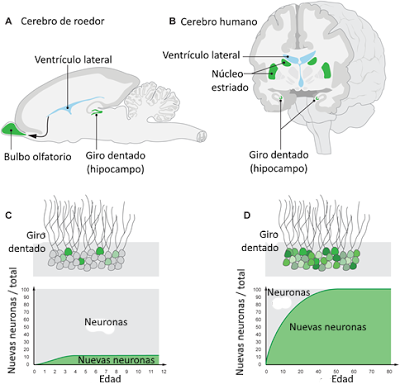 En humanos también se da neurogénesis en el núcleo estriado, región que no presenta esta característica en otras especies. Se desconoce la función biológica de estos procesos de regeneración, aunque parece que esta zona está relacionada con la "flexibilidad cognitiva", la capacidad de reajustar nuestros objetivos ante los cambios en el contexto, así como con el comportamiento social, la planificación y la modulación del movimiento, la recompensa, la motivación y el placer o la valoración del arte, especialmente de la música.
En humanos también se da neurogénesis en el núcleo estriado, región que no presenta esta característica en otras especies. Se desconoce la función biológica de estos procesos de regeneración, aunque parece que esta zona está relacionada con la "flexibilidad cognitiva", la capacidad de reajustar nuestros objetivos ante los cambios en el contexto, así como con el comportamiento social, la planificación y la modulación del movimiento, la recompensa, la motivación y el placer o la valoración del arte, especialmente de la música.