 2015 acabó con una buena noticia. Se acababa de completar el séptimo período de los elementos de la tabla periódica con el descubrimiento de cuatro elementos químicos nuevos (que incluso lograron una amplia cobertura en los principales medios de noticias y blogs de química). La IUPAC (International Union of Pure and Applied Chemistry o Unión Internacional de Química Pura y Aplicada en castellano) dio la noticia el 31 de diciembre de 2015 [1].
2015 acabó con una buena noticia. Se acababa de completar el séptimo período de los elementos de la tabla periódica con el descubrimiento de cuatro elementos químicos nuevos (que incluso lograron una amplia cobertura en los principales medios de noticias y blogs de química). La IUPAC (International Union of Pure and Applied Chemistry o Unión Internacional de Química Pura y Aplicada en castellano) dio la noticia el 31 de diciembre de 2015 [1].
Estos elementos nuevos ocupan el número Z=113 para el descubierto por “RIKEN” en Japón [2], los números Z=115 y Z=117 para los descubiertos conjuntamente por los laboratorios “Joint Institute for Nuclear Research” en Dubna, Rusia; “Lawrence Livermore National Laboratory” en California, EE.UU. [3,4], y el “Oak Ridge National Laboratory” en Oak Ridge, Tennessee, EE.UU y para el número Z=118 para el descubierto conjuntamente por los laboratorios “Joint Institute for Nuclear Research” en Dubna, Rusia y el “Lawrence Livermore National Laboratory” en California, EE.U.U.
Pero, ¿qué es lo que sabemos acerca de estos nuevos elementos?. Continua leyendo…

fig. 1, imagen interna de acelerador de partículas
Lo primero que sabemos es como se crearon, ya que son elementos que no se encuentran en la naturaleza y son artificiales o sintéticos y solo pueden crearse en laboratorios, pero no en cualquier laboratorio. Para crearlos, se bombardean en aceleradores de partículas unos átomos con otros con el fin que sus núcleos se fusionen, cosa que es un proceso arduo, ya que se ha de dotar a los proyectiles de una velocidad descomunal y han de impactar contra el blanco con el ángulo correcto. El problema de este proceso es que muy pocos impactos en realidad tienen la velocidad correcta y la orientación que conduzca a la fusión de los dos elementos y crear un nuevo elemento. De hecho, “muy pocos” es probablemente una especie de eufemismo (tal vez sólo un impacto en unos cuantos miles de millones realmente tiene éxito en la creación del nuevo elemento deseado), ya que la mayoría de las colisiones o bien dan lugar a la desviación de los dos átomos, o la completa aniquilación de ambos.
Elementos químicos superpesados y la “isla de estabilidad”
Los elementos químicos más allá de número atómico 104 se conocen como elementos superpesados. Aunque los elementos superpesados no se han encontrado en la naturaleza (a excepción de algún indicio del elemento 122 o eka-thorio [5]), pueden ser producidos mediante la aceleración de haces de núcleos ligeros y disparándolos contra otros más pesados como núcleos blanco. La fusión entre estos dos núcleos en ocasiones produce un elemento químico superpesado que por lo general, sólo existen por un corto tiempo.
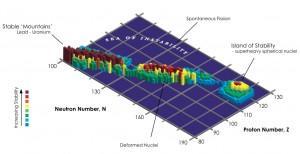
fig 2, los modelos matemáticos predicen una isla de estabilidad allá por el elemento 120
El descubrimiento de estos elementos superpesados acerca más a los científicos a la llamada “isla de estabilidad”, un término de la física nuclear que se refiere a la posible existencia de una región más allá de la tabla periódica que conocemos donde los nuevos elementos superpesados con números especiales (números mágicos) de neutrones y protones exhibiría una mayor estabilidad (de horas o incluso semanas). La existencia de dicha isla extendería la tabla periódica de los elementos a elementos aún más superpesados y permitiría experimentos químicos con ellos. Dicha isla de estabilidad se cree que comienza para el elemento con 120 protones en el núcleo.
Incluso cuando se producen con éxito estas colisiones, los elementos superpesados creados son tremendamente inestables y se desintegran radiativamente en otros elementos menos pesados que ellos hasta que al final por lo general se desintegran por una fisión espontánea.
La serie de números mágicos es la siguiente: 2, 8, 14, 20, 28, 32 [6], 50, 82, 126, 184, …, por lo que a los elementos con combinación de dos de ellos se le conoce como doblemente mágicos, como ocurre con los siguientes isótopos:
4He, con 2 protones y 2 neutrones; 16O, con 8 protones y 8 neutrones; 40Ca, con 20 protones y 20 neutrones; 48Ca, con 20 protones y 28 neutrones; 208Pb, con 82 protones y 126 neutrones. Con estos datos es probable que el próximo isótopo doblemente mágico sea el 310Ubh ( eka-plutonio) con 126 protones y 184 neutrones en su núcleo.
Estos isótopos tienen una estabilidad especial por lo que su abundancia es mayor al resto de los isótopos de los elementos.
¿Qué sabemos de estos nuevos elementos químicos?
Como sólo existen para la mínima fracción de un segundo, es difícil saber mucho acerca de estos nuevos elementos. Solo podemos especular en como se comportarían por la periodicidad de la tabla periódica, pero ni siquiera podemos decir con certeza si son sólidos, líquidos o gases a temperatura ambiente esta que es probable que todas sean sólidos.
Tampoco sabemos sus nombres todavía. Por ahora son Ununtrium, ununpentium, ununseptium y ununoctium desde que en 2002 la IUPAC decidiera nombrarlos así [5] hasta que se pusiera un nombre definitivo y reconocido mundialmente ( un símbolo, claro está). Una vez se han descubierto estos elementos los descubridores oficiales de los elementos serán invitados por la IUPAC para sugerir nombres y símbolos, siguiendo una serie de reglas.
Veamos como los formaron:
El elemento 113 o ununtrium
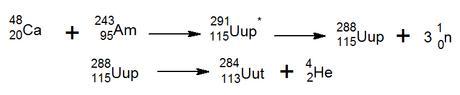
Realmente el primer indicio de la existencia del elemento 113 (el isótopo con una masa de 284 y una vida útil de alrededor de 1 segundo) fue registrado por el ICIN en 2003 cuando bombardearon con el isótopo 48Ca el isótopo 243Am, obteniendo el elemento 288Uup (elemento 115). Este nuevo elemento se desintegraba por perdida un núcleo de helio (desintegración alfa) por lo que se formaba el isótopo 284Uut (elemento 113), con una vida media de un segundo.
 El elemento 115 o ununpentium
El elemento 115 o ununpentium

En febrero de 2004 se informó en la prestigiosa revista Physical Review C que un equipo integrado por científicos rusos en el Joint Institute for Nuclear Research y los científicos norteamericanos del Lawrence Livermore National Laboratory descubrieron el unumpentio. Para ello bombardearon con 48Ca nucleos de 243Am, con lo que produjeron 4 átomos de ununpentium (ver elemento 113). Estos núcleos nuevos se desintegraban en cuestión de 100 milisegundos por emisión alfa (núcleos de helio) al elemento 113 (ununtrium). En 2013, un laboratorio independiente confirmó este hallazgo.
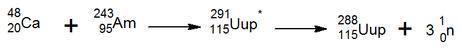 El elemento 117 o ununseptium
El elemento 117 o ununseptium
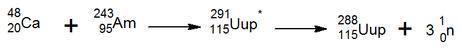
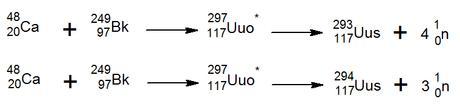
Entre junio de 2009 y enero del 2010 los científicos del Joint Institute for Nuclear Research ruso anunciaron que habían detectado con éxito la desintegración de un nuevo elemento con número atómico 117, concretamente de dos isótopos que se desintegraban mediante radiación alfa (núcleos de He) antes de una fisión espontánea. Para ello bombardearon una fina lámina de 249Bk con núcleos de 48Ca. Según el informe oficial publicado el 9 de abril de 2010 en la prestigiosa revista Physical Review Letters, dichos isótopos eran el 294Uus y el 293Uus, formados como sigue a continuación:
 El elemento 118 o ununoctium
El elemento 118 o ununoctium

El primer grupo de átomos de ununoctio fue propiamente observado en el Joint Institute for Nuclear Research de Dubna, Rusia, en 2002, y cuatro años mas tarde, en octubre de 2006 un equipo conjunto del Joint Institute for Nuclear Research y del Lawrence Livermore National Laboratory anunciaron que habían detectado indirectamente un total de tres o quizás cuatro núcleos de 294Uuo, solo uno o dos en 2002 y dos más en 2005, mediante la colisión de iones de 249Cf con 48Ca:

Conclusiones
Es posible que nos preguntemos la motivación científica para trabajar en el descubrimiento de nuevos elementos con nula utilidad debido a su ínfima existencia (del orden de milisegundos o menos) antes de transformarse en otros que ya conocemos. Tenemos que pensar que si las teorías son ciertas, en un futuro no muy lejano se llegue a sintetizar algún isótopo de los que se encuentren en la “isla de estabilidad” y este es el motivo principal que mueve a los científicos.
Referencias y fuentes de datos
[1] Discovery and Assignment of Elements with Atomic Numbers 113, 115, 117 and 118
[2] It’s official! Element 113 was discovered at RIKEN
[3] ORNL on team officially recognized for elements 115, 117 discovery
[4] Открытие новых химических элементов с номерами 113, 115, 117 и 118
[5] Naming of new elements(IUPAC Recommendations 2002)
[6] Un experimento del CERN revela un nuevo número mágico en un núcleo atómico
