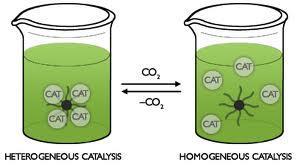
Catálisis homogénea
La oxidación del dióxido de azufre usando monóxido de nitrógeno como catalizador es un ejemplo de un catalizador homogéneo.
Un catalizador homogéneo se encuentra en la misma fase que los reactivos. Por ejemplo en la síntesis de ácido sulfúrico todas las especies químicas se encuentran en fase gaseosa.
Otro ejemplo ocurre durante la oxidación del talio (I) a talio (III) mediante cerio (IV) qie se reduce a serio (III) en solución acuosa.
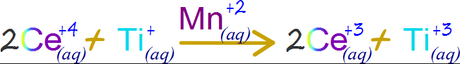
La reacción no catalizada es extremadamente lenta, posiblemente debido a que requiere el choque de tres iones positivos “los cuales naturalmente tendería a repelerse debido a sus cargas”.
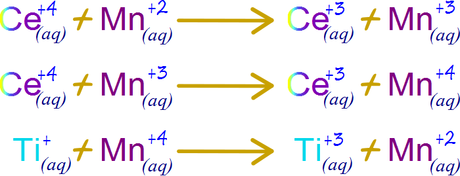
La adición del catalizador magnesio permite una ruta de reacción en la que cada uno de los tres pasos involucra solamente dos iones en el choque efectivo y no tres.
PRINCIPAL
REGRESAR