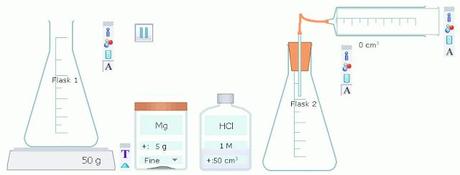
 Determinación experimental de las tasas de reacción
Introducción a la determinación experimental de las tasas de reacción.
Determinación por puntos de la tasa de la reacción promedio.
Determinación continua de la tasa de la reacción instantánea.
Determinación experimental de las tasas de reacción
Introducción a la determinación experimental de las tasas de reacción.
Determinación por puntos de la tasa de la reacción promedio.
Determinación continua de la tasa de la reacción instantánea.
Determinación continúa de la tasa de la reacción instantánea.
Existen metodologías más convenientes, dado que entre más puntos en el tiempo mejoran la resolución de este ejercicio, un método para obtener una curva continua eliminaría cualquier rastro de duda sobre el modo en que se comporta la curva de la reacción.
Estas metodologías son fundamentalmente físicas y permiten determinar la curva de concentraciones tanto para reacciones rápidas como para reacciones lentas.
Un ejemplo es la presión.
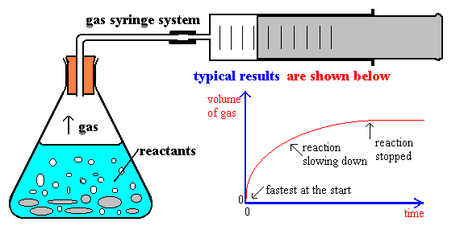
Figura DCR-01. Si tenemos una reacción que produce gases, es posible crear un sistema que sea capaz de determinar el valor de la presión de manera continua para todos los puntos dentro de un intervalo de tiempo.
Existen reacciones químicas que se llevan a cabo en fase gaseosa, y las propiedades de los gases pueden emplearse para determinar la tasa en que se ejecuta una reacción. Cabe recordar que los gases determinan su cantidad de sustancia mediante la ley de los gases “ideales o reales”.Si se tiene por ejemplo una reacción en fase gaseosa en la cual un gas se desdobla en dos gases puede emplearse la ley de Dalton para la presión combinada de los gases para poder seguir el incremento de cantidad de producto de manera indirecta.
Reacciones de color
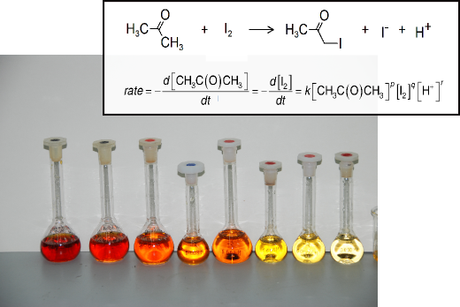
Figura DCR-02. El método de color puede emplearse para obtener datos de manera continua como discreta, y se basa en la determinación cuantitativa del cambio de color de un sistema mediante el uso de un espectrofotómetro.
Otra propiedad física usada para seguir el progreso son las reacciones de color, o absorción de ciertas partes de la luz por algunas especies químicas. Consideremos por ejemplo la siguiente reacción
El ion hipoyodito absorbe en el extremo azul del sector electromagnético cerca del 400 nm.

También se puede seguir la progresión de la descomposición del N2O5 a partir de la intensidad del color rojo-café del producto NO2
En estos experimentos, la intensidad de absorción de una determinada longitud de onda son medidas mediante un adecuado espectrofotómetro, sea este visible, infrarrojo, de resonancia magnética entre otros. PRINCIPAL REGRESAR
