Equilibrio químico Introducción al equilibrio químico I Introducción al equilibrio químico II Equilibrios estáticos contra equilibrios dinámicos Estequiometria y equilibrio químico, parte I La constante de equilibrio químico Equilibrios químicos homogéneos y heterogéneos El uso de la constante de equilibrio Interpretación cualitativa de la constante de equilibrio Cinética y equilibrio Predicción de la dirección de la reacción Cálculo de concentraciones usando las constantes de equilibrio Principio de Le-Chatelier Problemas de equilibrio químico
Ejercicio de equilibrio químico 2.
A 40°C un recipiente de 400 ml contiene en equilibrio 0.4g de dióxido de nitrógeno y 1.6g de tetraóxido de dinitrógeno. Calcular la constante para la disociación a esta temperatura. Respuesta. 
Plan Determinar las concentraciones Escribir la expresión de la constante de equilibrio Reemplazar y calcular la constante de equilibrio.
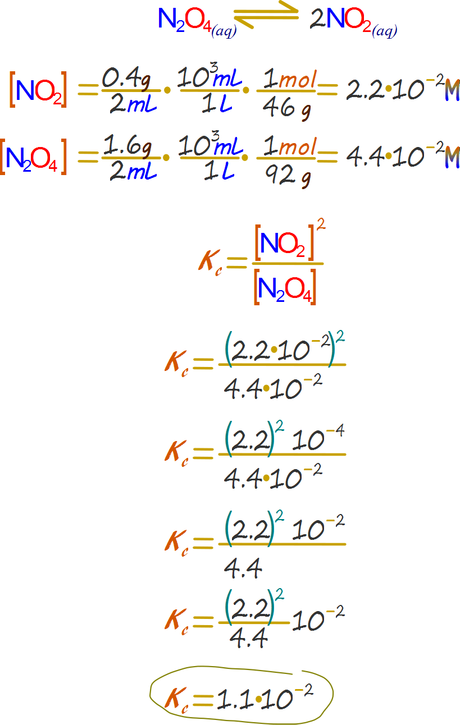
PRINCIPAL
REGRESAR
