 Hace prácticamente un año, a finales de 2015, aparecía la noticia que se habían descubierto cuatro nuevos elementos químicos (ver la entrada “4 nuevos elementos químicos, y ya son 118“). Unos meses más tarde, en junio, esos elementos ya tenían nombre (ver entrada “Los cuatro nuevos elementos ya tienen nombre“) por lo que el séptimo período de la tabla periódica ya estaba completo. El descubrimiento de estos elementos superpesados, o también llamados elementos superactínidos no deja de ser algo “sin utilidad” química, y pongo entre comillas lo de sin utilidad, pero sí tienen utilidad científica, al ser elementos con una vida media ínfima pero que nos acerca más a la hipotética isla de estabilidad que se encuentra más allá del elemento con 120 protones en el núcleo.
Hace prácticamente un año, a finales de 2015, aparecía la noticia que se habían descubierto cuatro nuevos elementos químicos (ver la entrada “4 nuevos elementos químicos, y ya son 118“). Unos meses más tarde, en junio, esos elementos ya tenían nombre (ver entrada “Los cuatro nuevos elementos ya tienen nombre“) por lo que el séptimo período de la tabla periódica ya estaba completo. El descubrimiento de estos elementos superpesados, o también llamados elementos superactínidos no deja de ser algo “sin utilidad” química, y pongo entre comillas lo de sin utilidad, pero sí tienen utilidad científica, al ser elementos con una vida media ínfima pero que nos acerca más a la hipotética isla de estabilidad que se encuentra más allá del elemento con 120 protones en el núcleo.
En esa primera entrada comenté también que por allá por 2008, un grupo de científicos liderados por el profesor Amnon Marinov, del Instituto de Física de Racah de la Universidad Hebrea de Jerusalen, habían descubierto un nuevo elemento superpesado con una masa atómica aproximada de 292, que correspondía con un núcleo de 122 protones y 170 neutrones al que llamaron eka-thorio o unbibium.
Todo empezó en la década de 1990, cuando el profesor Marinov observó unos fenómenos inexplicables relacionados con el descubrimiento de los estados isoméricos superdeformados e hiperdeformados de alto espín y de larga duración. Marinov intuía y esperaba que estos núcleos superpesados pudieran tener una semivida relativamente larga mientras estuvieran en esos estados isoméricos, y sí eso fuese así, podrían encontrarse en la naturaleza. Y se puso a buscar el la fuente natural más lógica (o una de las mas lógicas) donde poder encontrarlo, el torio.
El experimento de Marinov

Prof. Amnon Marinov, http://www.marinov-she-research.com/
Marinov estudió una muestra de torio natural mediante espectrometría de masa de campo de plasma acoplado inductivamente (ICP-SFMS). En este instrumento se introduce una solución del material a estudiar mediante una fuente de plasma de alta temperatura (6000-8000 K) donde a estas temperaturas predominan las especies atómicas. Los iones moleculares se producen principalmente por la interacción con el oxígeno y los iones de hidrógeno de la solución.
La máquina se calibró usando los isótopos 230Th, 235U y 238U y también las especies moleculares 238U16O (M = 254) , 232Th40Ar16O (M=288) y 238U40AR16O (M = 294) y se revisaron regularmente cada media hora a una hora de los experimentos y se corrigieron los datos en consecuencia. Entonces centran los estudios en la zona comprendida entre una masa de 291-293.
Marinov analizó diversas soluciones en tres sesiones, dando como resultado además del pico 238U40AR14N, se observan cuatro eventos en las proximidades de las masas predichas de los isótopos 292122 y 294122.
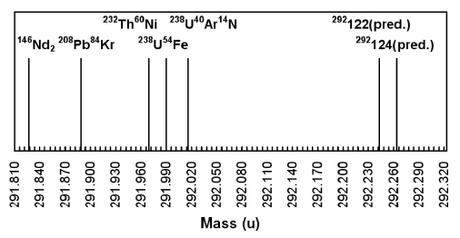
Fig. 1. representación del comportamiento sistemático de las masas de varias especies con M = 292 y los eventos detectados por Marinov.
La figura 1 presenta la suma de los 60 espectros. Marinov, sabiendo la concentración inicial de Th y el numero de conteos producidos, estimó que la concentración de la especie responsable de estos pico era de aproximadamente 1·10-12 de 232Th, o aproximadamente 1·10-16 de la solución. Estos eventos tampoco podía ser un nuevo isótopo de torio muy rico en neutrones, ya que este tendría una masa 292.399 u.
También predijo que la semivida previstas de su estado fundamental era del orden de 10-8 segundos y su concentración terrestre inicial era similar a la de 232Th, pero al tratarse de un estado isomérico superdeformado de alto espín, su vida media debería ser del orden de 108 a 139 año o de otro modo, se habría decaído.
Por desgracia, ninguno de estos hallazgos pudo ser confirmado por ningún otro grupo y sus afirmaciones de descubrimiento fueron universalmente desatendidas por la comunidad científica.
Núcleos superdeformados e hiperdeformados
En física nuclear, un número mágico es un número de nucleones de un núcleo atómico que le otorgan una mayor estabilidad al mismo frente a la desintegración nuclear, es decir, son más estables. Los números mágicos son los siguiente: 2, 8, 14, 20, 28, 50, 82, 126, 184, …, por lo que a los elementos con combinación de dos de ellos se le conoce como doblemente mágicos, como ocurre con los siguientes isótopos: 4He, con 2 protones y 2 neutrones; 16O, con 8 protones y 8 neutrones; 40Ca, con 20 protones y 20 neutrones; 48Ca, con 20 protones y 28 neutrones; 208Pb, con 82 protones y 126 neutrones. Con estos datos es probable que el próximo isótopo doblemente mágico sea el 310Ubh ( eka-plutonio) con 126 protones y 184 neutrones en su núcleo. En cierta medida, los números mágicos de protones se corresponden al máximo de la abundancia solar de elementos.
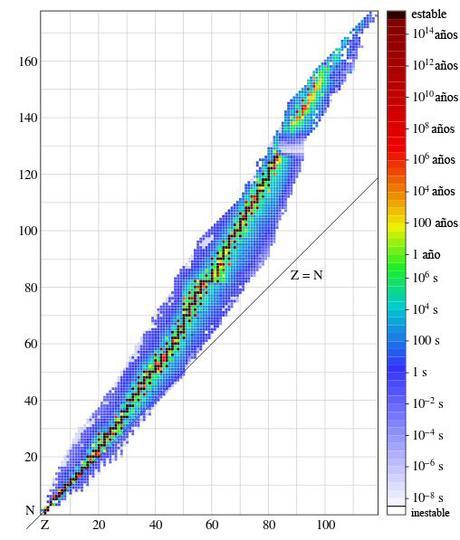
fig 2. vida media de los diferentes isótopos. En negro se aprecian los isótopos estables. Como vemos, cuando aumenta el número de protones, aumenta en mayor medida el número de neutrones.
Entonces, ¿por qué hay núcleos estables con números no mágicos de nucleones?. Para responder a esta pregunta tenemos que saber que es el espín nuclear.
El espín nuclear
El espín (del inglés spin ‘giro, girar’) es una propiedad física de las partículas elementales por el cual tienen un momento angular intrínseco de valor fijo. Electrones, neutrones y protones, los tres tipos de partículas que constituyen el átomo, tienen esta propiedad. Existe un momento angular asociado a la partícula misma ya se trate del electrón, protón y neutrón, y éste se describe mediante el número cuántico de espín que puede tomar valores de + ½ y –½.
En el núcleo atómico, cada protón se pueden aparear con otro protón con espín antiparalelo (algo análogo a lo que sucede con los electrones en los enlaces químicos). Los neutrones también pueden hacerlo. Por esta razón los núcleos con número de neutrones y protones impar dan lugar a un espín neto (diferente de cero), donde el número de desapareamientos contribuye con ½ al total del número cuántico de espín nuclear, denominado I. Así, los isótopos con I = 0 son inactivos a la RMN, los isótopos con I= 1/2 tienen una distribución esférica de carga en el núcleo mientras que los isótopos con I >= 1 no tienen una distribución de carga esférica en el núcleo, son cuadrupolares. Cuando I no es nulo, el núcleo tiene un momento angular de espín y un momento magnético asociado , µ, que depende de la dirección del espín.
- número de protones par:
- número de neutrones par: Suma protones + neutrones = par, por tanto el espín =0.
- número de neutrones impar: suma protones + neutrones = impar, por tanto el espín = 1/2.
- número de protones impar:
- número de neutrones par: suma protones + neutrones = impar, por tanto el espín >= 1
Rotación del núcleo
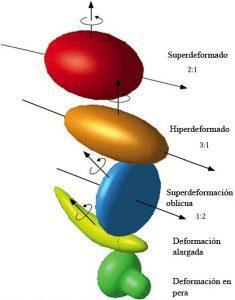
Fig 3. principales deformaciones de los núcleos
Los núcleos atómicos rotan sobre sí mismos y presentan un momento angular. Este momento angular depende del número cuántico I (número cuántico del momento angular o espín nuclear), que puede tomar diferentes valores dependiendo del tipo de núcleo, I=0, 1/2, 1, 3/2, 2, 5/2, 3, etc.
Hasta este momento hemos supuesto que el núcleo tiene una forma esférica, sin embargo esto no deja de ser una aproximación, por lo que resulta necesario conocer cual es la forma geométrica que tiene porque ¿qué pasa cuando el núcleo tiene I diferente de 0?
Para empezar, dado que la interacción fuerte (la que impera dentro del núcleo y mantiene unidos a los protones y los neutrones) conserva la paridad, impone ciertas restricciones a la geometría que puede tener un núcleo (ya que esta geometría debe conservar esta simetría). Así, cuando un núcleo no es esférico, solo puede tomar ciertas formas como las mostradas en la figura 3 (formas deformadas), aunque todas ellas son simétricas en al menos un eje de rotación.
Estabilidad de los estados superdeformados e hiperdeformados
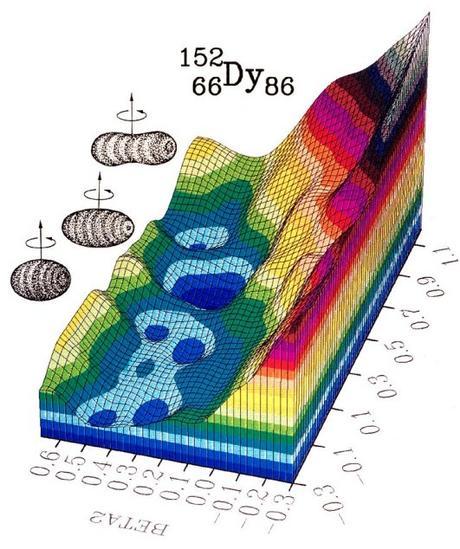
Atendiendo a esta regla, ¿qué pasa con lo núcleos estables que se encuentran entre dos números mágicos, y por tanto no son esféricos?. Podríamos pensar que no son estables pero como sabemos sí los son. Mirando la siguiente figura:
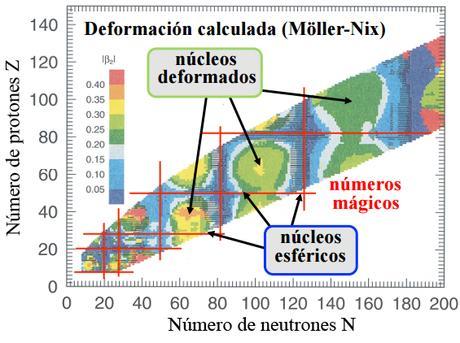
Vemos que los núcleos entre números mágicos de encuentran deformados, y además se encuentran más deformados cuanto mas alejados estén de un número mágico, llegando a ser superdeformados e hiperdeformados. Con este hecho, los científicos han supuesto que los núcleos superdeformados e hiperdeformados (con un número determinado de neutrones y protones en el núcleo) le confieren una estabilidad extra en comparación con sus isótopos vecinos. Un ejemplo de esto lo vemos en el disprosio, donde el valor más estable (eje z del gráfico, es decir, colores azules) corresponde a una geometría superdeformada y no a una geometría mas esférica. También la geometría hiperdeformada presenta más estabilidad que otras geometrías vecinas.
Referencias y fuentes de datos
Search for a superheavy nuclide with A = 292 and neutron-deficient thorium isotopes in natural thorianite
Researchers claim to have seen an element with an atomic number of 122, but some are sceptical.
Electronic structure of eka-thorium (element 122) compared with thorium
Shape deformations in atomic nuclei
Fenómenos sorprendentes en núcleos exóticos (y núcleos en condiciones exóticas)
Elucidación estructural: espectrometría de masas (Introducción)
NOTA: Si alguien necesita algún texto completo puedo pasárselo por correo electrónico
