Una mezcla en equilibrio gaseosa contiene 0.3 moles de monóxido de carbono, 0.1 moles de hidrógeno gaseoso, 0.02 moles de agua y una cantidad desconocida de metano.
En equilibrio esta mezcla posee una constante de 3.92 a 1200°C. El volumen del reactor es de 1 L.
La fórmula balanceada es la siguiente.

Análisis:
En este caso no conocemos el estado inicial de la reacción, por lo que no se puede emplear la tabla de cambios. Se debe emplear un reemplazo de las variables y constante conocidas y despejar la ecuación. Como se tiene un reactor de 1 L al realizar la conversión a molaridad solo cambia la unidad mas no la magnitud.
Reemplazar y calcular.
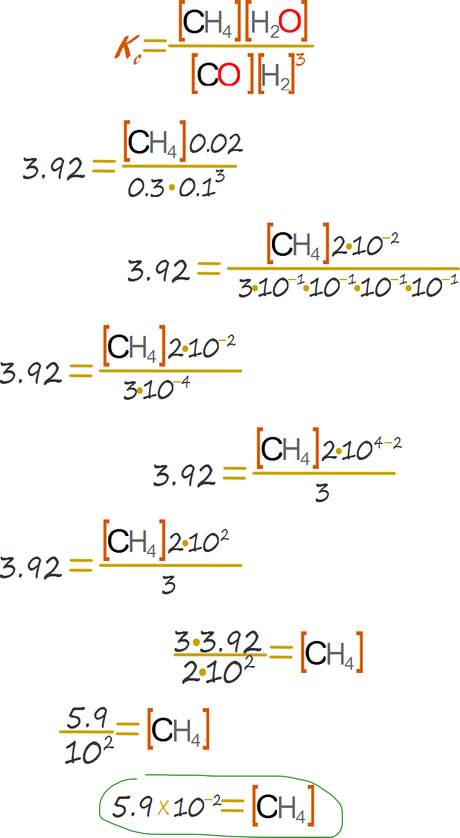
PRINCIPAL
REGRESAR
