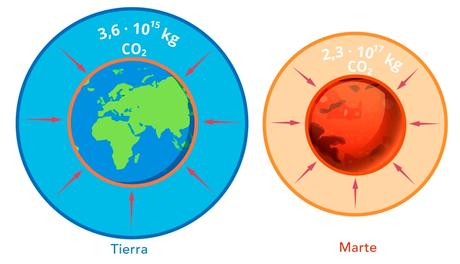
Existe una manera más o menos sencilla de calcular aproximadamente la cantidad de CO2 en la atmósfera conociendo su concentración atmosférica. Periódicamente aparecen noticias alarmantes sobre el incremento de esta concentración en partes por millón. A continuación veremos cual es la concentración en partes por millón y su equivalente en kilogramos de CO2 en la atmósfera. No olvidemos que estoy realizando un cálculo aproximado.

Características de la Tierra y la Atmósfera
Con el fin de calcular la cantidad de CO2 atmosférico se necesitan algunas variables que afectan al sistema Tierra-Atmósfera, partimos inicialmente con tres variables: la presión atmosférica, la densidad del aire, el diámetro de la Tierra y la aceleración de la gravedad terrestre.
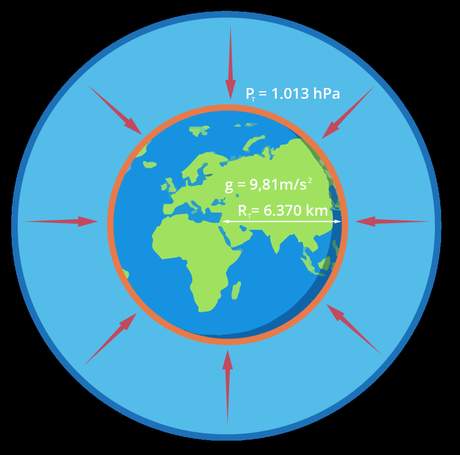
Donde el radio de la Tierra RT es de 6.370 km, la aceleración de la gravedad terrestre g es 9,81 m/s2 y la presión al nivel del mar PT adquiere un valor de 1.013 hPa (hecto Pascales), donde hecto es el prefijo de cien.
El valor de la presión de la atmósfera a nivel del mar no es nada más que el efecto del peso de la atmósfera sobre la superficie terrestre. Equivalente a la fuerza que ejerce la atmósfera sobre la Tierra.
Cálculo cantidad CO2 en la atmósfera Terrestre
De acuerdo con estas definiciones anteriores obtenemos las siguientes ecuaciones para la fuerza de la atmósfera sobre la Tierra, donde Mates la masa de la atmósfera terrestre que queremos calcular
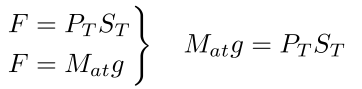
Observamos que se puede calcular la masa de la atmósfera terrestre Mat de la siguiente manera
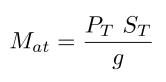
La superficie de la Tierra corresponde a la superficie de una esfera de radio terrestre, así
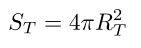
Finalmente la masa de la atmósfera terrestre la calculamos a partir de la siguiente ecuación
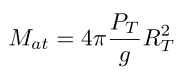
Colocando los valores numéricos obtendremos la masa atmosférica en kilogramos
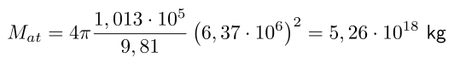
Así pues la atmósfera terrestre tiene una masa de 5,26 trillones de kilogramos. Veamos a continuación cuántos de estos kilogramos corresponden al CO2.

A continuación debemos calcular el volumen de la atmósfera. Dado que el volumen (m³) y la masa (kg) se encuentran relacionadas mediante la densidad (ρ).
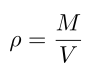
Conocemos que la densidad media de la atmósfera (aire) es de 1,2 kg/m³. Así podemos calcular el volumen de la atmósfera de la siguiente manera
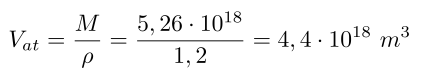
Veamos a continuación cuantos de estos m³ corresponden a kilogramos de CO2. Para realizar el cálculo supongo una concentración de 415 ppm, que significa una concentración relativa de 415 partes de CO2 por millón de aire, que corresponde mas o menos a la concentración actual.
Esto quiere decir que podemos calcular la concentración de las siguientes maneras, todas ellas son equivalentes.
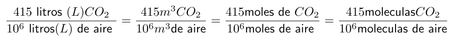
Dado que queremos obtener la cantidad de kilogramos de CO2 nos es más útil la relación entre los moles de dióxido de carbono y moles de aire. Para realizar el factor de conversión tenemos que conocer primero el peso molecular del dióxido de carbono y cuanto ocupa un mol de aire.
La molécula de CO2 está formada por dos átomos de oxigeno (O) y un átomo de carbono (C), en la siguiente configuración

Necesitamos calcular su masa molecular, para ello conocemos que la masa atómica de un átomo de carbono es 12,01 u (unidades de masa atómica) y la masa atómica de un átomo de oxígeno es 16 u. Entonces la masa molecular del dióxido de carbono será
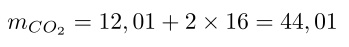
Conviene subrayar que este resultado significa que 1 mol de dióxido de carbono tiene una masa de 44,01 g. Otra condición que aplico es considerar el aire como un gas ideal, entonces 1 mol de aire ocupa 22,4 litros.
Finalmente aplicando las condiciones anteriores se establecen las siguientes relaciones
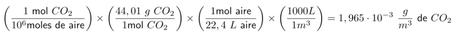
De donde resulta que podemos establecer el resultado deseado
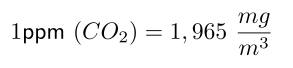
Aplicamos ahora el volumen calculado de la atmósfera terrestre y obtendremos los kilogramos de dióxido de carbono que corresponden a una concentración de 1ppm.
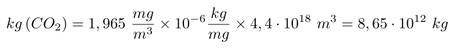
Si consideramos una concentración actual de 415 ppm, obtendremos la cantidad de kilogramos en la atmósfera actual.
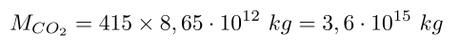
Como resultado obtenemos que en la atmósfera actualmente hay una cantidad de 3,6 mil billones de kilogramos de CO2, que corresponden a 3,6 billones de toneladas de CO2
Concentración en el Cámbrico
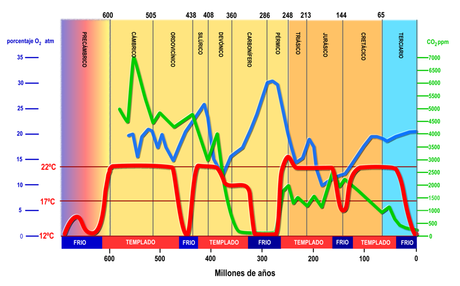
En el período Cámbrico, hace unos 500 millones de años la concentración de dióxido de carbono alcanzó la cifra de 7000 ppm (ver la gráfica al final del post), que corresponden a la cantidad de kilogramos siguiente
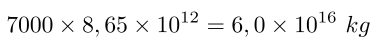
Que corresponden a 60 billones de toneladas de CO2.
La concentración de dióxido de carbono en la atmósfera fue disminuyendo y concentrándose en el subsuelo terrestre y los océanos, hasta llegar a una concentración atmosférica muy baja, menor que la actual en el Carbonífero. Los combustibles fósiles como el carbón y el petróleo proceden precisamente del período Carbonífero de hace unos 350 millones de años.
Concentración en el Jurásico
Durante el período Jurásico la concentración alcanzo el valor de unos 2500 ppm, que corresponden a unos 22 billones de toneladas de CO2. Desde entonces la concentración ha ido disminuyendo hasta el valor actual. Por supuesto el CO2 no ha desaparecido sino que se encuentra enterrado en el subsuelo y en los océanos.
Comparación emisión CO2 coches.
Según los datos que se estipulan actualmente aproximadamente un millón de coches liberan una cantidad de 4,9 millones de toneladas de CO2 al año. Calculemos qué tanto por ciento representa respecto la concentración atmosférica.
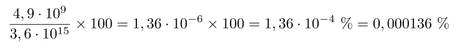
Es decir el 0,000136 por ciento.
Cálculo cantidad CO2 en la atmósfera Marciana
Las características de Marte se muestran en la siguiente imagen donde podemos apreciar que su radio Rm es de 3.390 km, la gravedad marciana ges de 3,711 m/s2 y la presión de su atmósfera sobre la superficie marciana es de 0,636 kPa.
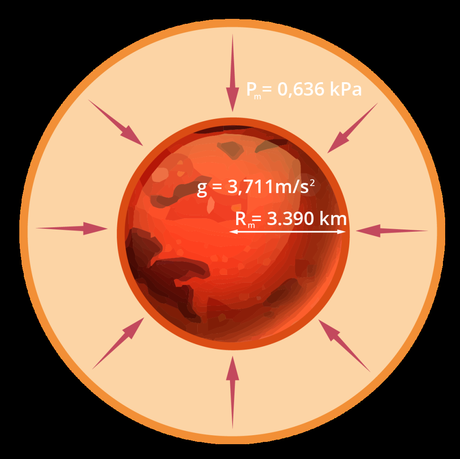
Escogemos la fórmula anterior para la masa de la atmósfera terrestre y aplicamos los valores del planeta Marte.
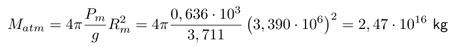
La densidad de su atmósfera marciana es de 0,020 kg/m³, de donde se obtiene el volumen
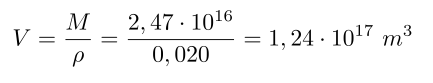
La composición de la atmósfera marciana es básicamente dióxido de carbono, con una concentración del 95 %, así podemos calcular
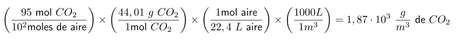
Así pues la cantidad de dióxido de carbono en la atmósfera marciana será
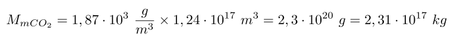
que corresponde a 231 mil billones de kilogramos de CO2 o 230 billones de Toneladas de CO2.