
Manejo de datos en una titulación de ácido base: cálculos teóricos
Esta fase es importante, pero no se debe sobreestimar. Y a sobreestimar me refiero a procesar todos los datos de la tabla uno por uno con este método, debido a que así nunca terminarían, ¡NUNCA!
Dado lo anterior en esta fase del procesamiento de datos lo que se busca es:
1- Procesar un dato promedio entre todos. 2- Mediante este dato realizar el procesamiento para observar si existe una coincidencia de magnitudes con el valor teórico al cual debemos aproximarnos.
Dicho lo anterior tenemos el siguiente problema. Se extrajo un volumen A ml de ácido clorhídrico al 37% y se lo diluyó hasta un volumen de 1 L de agua destilada. Posteriormente se extrajeron alícuotas de D ml para estandarizar. Para la titulación se empleó una solución patrón de hidróxido de sodio formado al diluir B g de hidróxido de sodio en C ml de agua destilada. Cuando se realizó la titulación se obtuvo un volumen E ml de hidróxido de sodio consumido. El punto final de la titulación se hizo con el indicador Z que marcó un determinado pH.
Si lo se, es algo raro usar letras en lugar de números, pero esto lo hago para poder abarcar mas casos, en cualquier caso el procedimiento se describe aquí (Enlace →).
(Objetivo: corroborar que la solución de ácido clorhídrico esté al 37%)
Paso 1. Determinar la concentración molar del hidróxido de sodio. Paso 2. Determinar los moles reales consumidos durante la titulación. Paso 3. Determinar la concentración de la solución de ácido en el Erlenmeyer al final de la titulación. Paso 4. Determinar los moles reales de ácido en el volumen final de la solución titulada. Paso 5. Determinar los moldes del ácido de la alícuota. Paso 6. Determinar la molaridad de la solución de 1 L. Paso 7. Determinar los moles reales en la solución de 1 L Paso 8. Determinar la concentración de la solución A. Paso 9. Expresar la respuesta en porcentaje en peso.
Paso 1. Determinar la concentración molar del hidróxido de sodio.
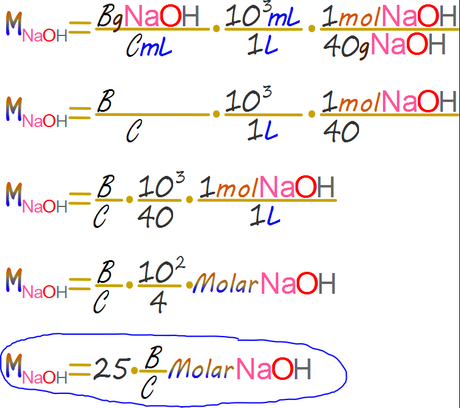
Paso 2. Determinar los moles reales consumidos durante la titulación.
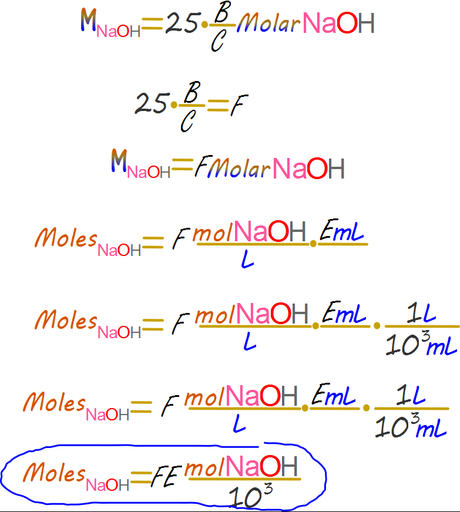
Paso 3. Determinar la concentración de la solución de ácido en el Erlenmeyer al final de la titulación.
Debido a que tratamos con ácido fuerte que se disocia totalmente se emplean como sinónimo ácido y protones. En este punto es donde el pH del indicador "que es fenolftaleina generalmente" se vuelve importante.
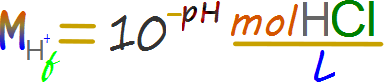
Paso 4. Determinar los moles reales de ácido en el volumen final de la solución titulada.
El volumen final de la solución titulada es el volumen de la alícuota D más el volumen consumido por la bureta E.
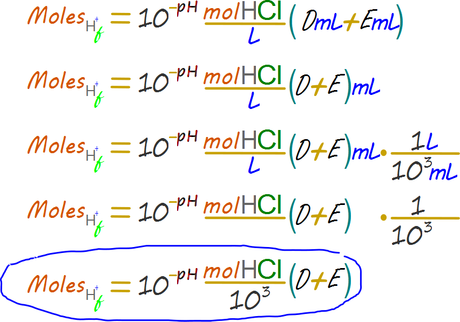
Paso 5. Determinar los moles del ácido de la alícuota.
Aquí es donde el volumen de la bureta se hace relevante. El volumen de la bureta representa el cambio en la concentración de iones hidrogeniones de la alícuota hasta llegar a los valores finales.
En este paso debemos emplear la ecuación balanceada para determinar la relación estequimétrica del hidróxido, el hidroxilo y el ácido.

El hidróxido produce un grupo hidroxilo que reacciona 1:1 con los protones del ácido clorhídrico.
Lo anterior implica que los moles consumidos de ácido clorhídrico son los mismos moles que se consumieron de hidróxido de sodio.
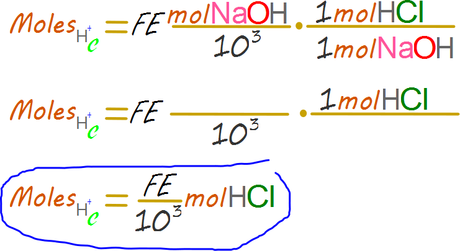
Los moles iniciales de la alícuota se obtienen sumando los moles finales de protones y los moles consumidos del ácido, es decir, una suma.
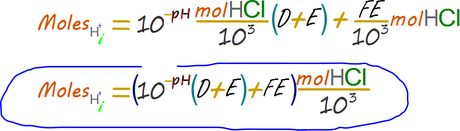
Paso 6. Determinar la molaridad de la solución de 1 L.
Finalmente la cantidad de protones en la alícuota original es igual a la suma de la cantidad de protones remanente en la solución al final de la titulación más la cantidad de protones que se consumió en la reacción.
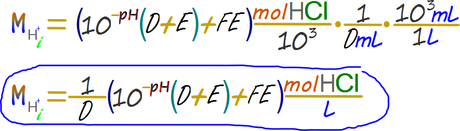
Paso 7. Determinar los moles reales en la solución de 1 L
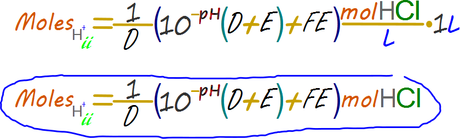
Paso 8. Determinar la concentración de la solución original
El volumen contenido en la pipeta (cantidad A) original empleada para extraer la solución de ácido al 33% del frasco original traspaso un volumen menor pero con la misma concentración, por lo cual dividir los moles que tenemos entre el volumen extraído con la pipeta nos dará la concentración original.
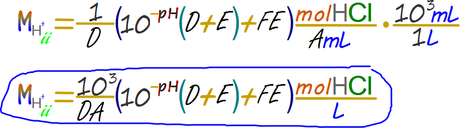
Paso 9. Expresar la respuesta en porcentaje en peso.
Se requiere la densidad del ácido clorhídrico, aunque varía con la presión, la temperatura y la concentración, los valores de la densidad rondan este valor
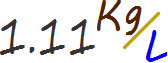
Ejecutamos el factor de conversión
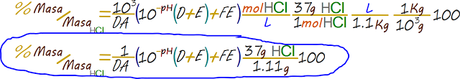
Divertido ¿no?, en efecto la titulación es un procedimiento interesante pero muy complejo si no se da una guía adecuada. Por lo general las prácticas de laboratorio solo exigen llegar hasta el paso 6 y con ella se efectúa la comparación estadística. Debido a esto, el análisis más práctico con tablas de Excel lo haremos solo hasta el paso 6. Un detalle adicional, los cálculos expuestos aquí son válidos para cualquier ácido y base fuerte que liberen un solo protón y un solo electrón respectivamente. PRINCIPAL
REGRESAR
